আসসালামু আলাকুম,
এসএসসি ২০২১ সালের শিক্ষার্থী বন্ধুরা,
আশা করি সবাই ভালো আছেন সুস্থ আছেন।
সেই কামনাই করি।
বরাবরের মতো আজকের পোস্টও ২০২১ সালের এসএসসি পরীক্ষার্থীদের জন্য দেওয়া এসাইনমেন্ট প্রশ্ন ও একটি নমুনা উত্তর লিখে দিব।
নমুনা উত্তর হুবুহু না লিখে ধারণা নিয়ে লেখার অনুরোধ রইলো
ভুলত্রুটি থাকলে ক্ষমা দৃষ্টিতে দেখবেন।
রসায়ন (নং-১) প্রশ্ন
প্রতিকের পাশে উল্লিখিত ভরসংখ্যা বিশিষ্ট মৌলের
নিউট্রন সংখ্যা, বাের পরমাণু মডেল অনুসারে পরমাণুর গঠনের চিত্র শক্তিস্তরে ইলেকট্রন বিন্যাস এবং উপশক্তিস্তরে (অরবিটালসমূহে) -ইলেকট্রন বিন্যাস
সংশ্লিষ্ট প্রতিবেদন।
Na(11), ভরসংখ্যা- 23
P (15), ভরসংখ্যা-31
k (19), ভরসংখ্যা-40
Cu (29), ভরসংখ্যা-63
তারিখ : ১৮ ই জুলাই, ২০২১
বরাবর,
প্রধান শিক্ষক
মডেল একাডেমী
মিরপুর, ঢাকা
বিষয়-প্রতিকের পাশে উল্লিখিত ভরসংখ্যা বিশিষ্ট মৌলের
নিউট্রন সংখ্যা, বাের পরমাণু মডেল অনুসারে পরমাণুর গঠনের চিত্র শক্তিস্তরে ইলেকট্রন বিন্যাস এবং উপশক্তিস্তরে (অরবিটালসমূহে) -ইলেকট্রন বিন্যাস
সংশ্লিষ্ট প্রতিবেদন।
সূত্র / স্বারক নং: ম, এ, ২০২১-৮ তারিখ: ১৮- “জুলাই, ২০২১
জনাব,
বিনীত নিবেদন এই যে, আপনার আদেন নং “ম:এ,২০২১
৮ তারিখ ১৮ ই জুলাই ২০২১ অনুসারে, প্রতীকের পাশে
উল্লেখিত সংখ্যা বিশিষ্ট মৌলের নিউট্রন সংখ্যা,
বোর পরাণু মডেল অনুসারে পরমানুর গঠন চিত্র, শক্তিস্তর এ ইলেকট্রন বিন্যাস এবং উপশক্তিস্তরে
(অরবিটালসমূহে) ইলেকট্রন বিন্যাস”-সংশ্লিষ্ট
প্রতিবেদনটি নিম্নে পেশ করছি।
ভরসংখ্যাবিশিষ্ট মৌলের নিউট্রন সংখ্যা,
বাের মডেল অনুসারে পরমানুর গঠন চিত্র, শক্তিস্তরে
ইলেকট্রন বিন্যাস এবং উপশক্তিস্তরে অরবিটালসমূহে)
ইলেকট্রন বিন্যাস ”
(ক)
নিউট্রন সংখ্যা নির্ণয়-
উল্লেখিত মৌল চারটি হল;
Na(11), ভরসংখ্যা- 23
P (15), ভরসংখ্যা-31
k (19), ভরসংখ্যা-40
Cu (29), ভরসংখ্যা-63
অমরা জানি, নিউট্রন সংখ্যা = “ভরসংখ্যা- প্রােটন সংখ্যা।
উদীপক হতে, Na এর ভরসংখ্যা 23 এবং
প্রােটন সংখ্যা 11
Na এর নিউট্রন সংখ্যা = 23-11
=12
P এর ভরসংখ্যা 31 এবং প্রােটন সংখ্যা 15
সুতরাং, p এর ভরসংখ্যা = 31–15
=16
k এর নিউট্রন সংখ্যা =40-19
=21
Cu এর ভর সংখ্যা 63 এবং প্রােটন সংখ্যা 29
সুতরাং, Cu এর নিউট্রন সংখ্যা = 63-29
= 34
(খ)
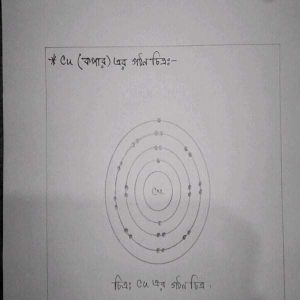
বাের মডেল অনুসারে পরমাণুর গঠনের চিত্র ;
উদ্দপকে উল্লেখিত মৌল চারটি হলো
Na(11), ভরসংখ্যা- 23
P (15), ভরসংখ্যা-31
k (19), ভরসংখ্যা-40
Cu (29), ভরসংখ্যা-63
বাের পরমাণু মডেল অনুসারে ইলেক্ট্রন নির্দিষ্ট
(বাকি অংশ লেখা সমস্যা হওয়ায় ছবি তুলে দিলাম)
(গ)
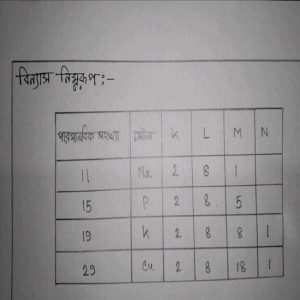
মৌলের শক্তিস্তরে ইলেক্ট্রন বিন্যাস –
বোর পরমাণু মডেল অনুসারে পরমাণুতে যে সকল ইলেকট্রন থাকে সেগুলো শুধু নির্দিষ্ট ব্যাসার্ধের কত অনুমোদিত বৃত্তাকার কক্ষপথে ঘুরে এই নির্দিষ্ট ব্যাসার্ধের অনুমোদিত বৃত্তাকার কক্ষপথে গুলো কে প্রধান শক্তি স্তর বলা হয় প্রতিটি প্রধান শক্তিস্তরে সর্বোচ্চ ইলেকট্রন ধারণক্ষমতা
2
2n,যেখানে n=
উপশক্তিস্তরে (অরবিটালল) ইলেকট্রন বিন্যাস :
আমরা জানি,
উপশক্তিস্তরের l দ্বারা চিহ্নিত করা হয়। আর এই
l এর মান 0 থেকে -1 পর্যন্ত। আবার উপশক্তিস্তর কে অরবিটাল বলা হয়। এই উপশক্তিস্তর বা অরবিটালগুলোকে sp,d,f দ্বারা প্রকাশ করা হয়।
এখানে n=1 হলে l=0 অরবিটাল একটি :1s
n=2 হলে l=0,1অরবিটাল দুইটি 2s,2p
n=3 হলে l=0,1,2 অরবিটাল তিনটি 3s,3p,3d
n=4 হলে l=0,1,2,3 অরবিটাল চারটি :4s,4p,4d,4f
প্রতিবেদনের বিষয়-
প্রতিবেদক এর নাম-
প্রতিবেদন লেখার সময়-
প্রতিবেদন জমার তারিখ-
প্রতিবেদক এর স্বাক্ষর-











ato pore lav ki auto pass e to dibo
Good
fine post
nice
good
Nice
বেশ ভালো পোস্ট।